Le chemin vers la rémission avec le mépolizumab dans l’asthme sévère : du ciblage de l’IL-5 aux preuves du monde réel
Suite aux nouvelles données concernant le mépolizumab dans la prise en charge thérapeutique de l’asthme sévère, la rédaction de La référence médicale a eu des entretiens passionnants avec trois experts : le professeur Guy Brusselle (UZ Gent), le professeur Florence Schleich (CHU Liège) et le professeur Lieven Dupont (UZ Leuven).

Leurs réflexions partagées, leurs expériences cliniques et leur interprétation scientifique ont servi de base à cet article, qui brosse un tableau clair et bien documenté du parcours complet du mépolizumab vers la rémission.
Mépolizumab : 9 ans d’expérience avec un traitement ciblant l’IL-5 dans l’asthme sévère
Le mépolizumab (Nucala), approuvé et remboursé en Belgique depuis 2016, a été le premier anticorps monoclonal à cibler spécifiquement l’interleukine-5 (IL-5). Il se lie à l’IL-5 et bloque son action. L’IL-5 joue un rôle crucial dans la croissance, la différenciation, l’activation et la survie des éosinophiles.4 Plusieurs études cliniques ont démontré l’efficacité du mépolizumab chez les patients atteints d’asthme sévère à éosinophiles : il diminue le nombre d’exacerbations d’asthme (étude MENSA)1 et réduit le besoin de corticostéroïdes oraux (étude SIRIUS).2 Les résultats de l’étude MUSCA ont montré qu’un traitement par mépolizumab s’accompagne également d’une amélioration de la qualité de vie, d’un meilleur contrôle de l’asthme et d’une fonction pulmonaire améliorée.3 De plus, le profil de sécurité du mépolizumab était favorable. Dans les études cliniques menées chez des patients atteints d’asthme sévère réfractaire à éosinophiles, les effets indésirables les plus fréquemment rapportés sous traitement étaient les céphalées (20 %), les réactions au site d’injection (8 %) et les douleurs dorsales (6 %).4
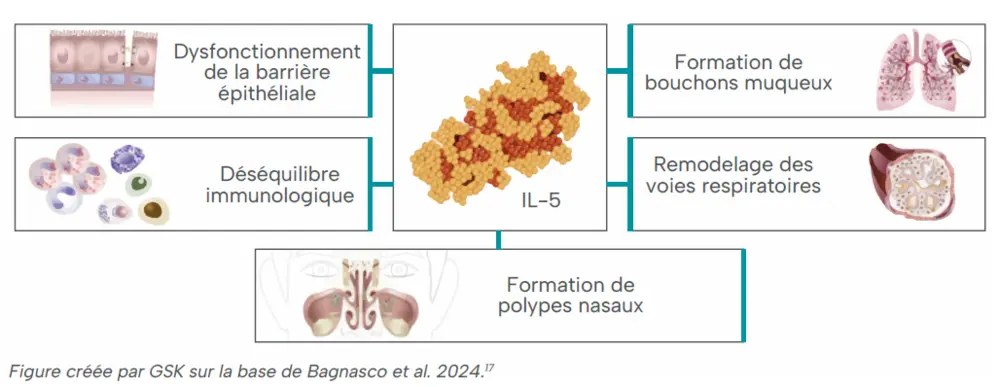
Figure 1. L’IL-5 joue un rôle central dans la régulation des processus pathologiques importants qui sous-tendent les maladies inflammatoires de type 2.17
Bien que les études contrôlées randomisées aient démontré l’efficacité et la sécurité du mépolizumab, les données du monde réel restent essentielles pour confirmer ces résultats dans une population plus large et plus diverse.5 L’étude REDES, réalisée chez 318 patients atteints d’asthme sévère à éosinophiles, a confirmé qu’un traitement par mépolizumab était également efficace dans la pratique quotidienne : au cours des 12 mois de traitement, une réduction des exacerbations de 77,5 %, une amélioration significative de la fonction pulmonaire et du contrôle de l’asthme et une diminution de l’utilisation de corticostéroïdes oraux ont été constatées. Il est intéressant de noter que ces avantages étaient indépendants des valeurs initiales des éosinophiles sanguins.6
L’IL-5 est plus qu’un modulateur des éosinophiles : c’est une molécule clé dans l’inflammation de type 2 7,17
IL’interleukine-5 (IL-5) joue un rôle central dans la pathogenèse des maladies inflammatoires de type 2. Traditionnellement, le rôle de l’IL-5 était attribué à la régulation des éosinophiles : elle stimule leur maturation, leur activation, leur migration et leur survie. Les traitements anti-IL-5 tels que le mépolizumab ont été développés pour inhiber cette inflammation médiée par les éosinophiles. Cependant, de nouvelles découvertes montrent que l’IL-5 va bien au-delà de l’activation des éosinophiles. L’IL-5 influence divers processus pathologiques qui contribuent à l’inflammation chronique, dont le dysfonctionnement de la barrière épithéliale, le déséquilibre immunitaire, la formation de bouchons muqueux, le remodelage des voies respiratoires et la formation de polypes nasaux (Figure 1).7,17
Plusieurs types de cellules sont concernés, comme les cellules épithéliales, les mastocytes, les basophiles, les plasmocytes, les neutrophiles, les fibroblastes et les cellules lymphoïdes innées de type 2. Ce profil d’action plus large de l’IL-5 offre un aperçu de l’efficacité des traitements anti-IL-5 dans des pathologies telles que l’asthme sévère à éosinophiles et la rhinosinusite chronique avec polypes nasaux (RSCaPN).4,7 Ces connaissances soutiennent l’utilisation des thérapies anti-IL-5 comme approche ciblée de l’inflammation de type 2 à plusieurs niveaux.7
Quelles nouvelles perspectives l’étude MESILICO offre-t-elle sur le potentiel du mépolizumab chez les patients atteints d’asthme sévère ?
Professeur Guy Brusselle : L’étude MESILICO confirme que le mépolizumab fait plus que supprimer l’inflammation éosinophilique. Dans cette étude chez des patients adultes atteints d’asthme sévère à éosinophiles d’apparition tardive, il a été démontré qu’un traitement anti-IL-5 par mépolizumab entraîne non seulement une amélioration clinique, mais aussi une réduction significative des changements structurels dans les voies respiratoires. Concrètement, après 12 mois de traitement, on a observé une nette diminution de l’épaisseur de la membrane sous-épithéliale, de la couche musculaire lisse et des lésions épithéliales, ainsi qu’une forte diminution du nombre d’éosinophiles tissulaires. Il est intéressant de noter que les récepteurs de l’IL-5 sont également exprimés sur les cellules épithéliales et les fibroblastes, ce qui explique comment l’IL-5 peut contribuer directement à un dysfonctionnement de la barrière et au remodelage des voies respiratoires. Cela est pertinent dans la pratique : les bouchons muqueux et les lésions épithéliales sont associés à une détérioration de la fonction pulmonaire. L’étude MESILICO démontre également qu’un traitement par mépolizumab peut améliorer ces facteurs, avec des effets favorables sur le taux de VEMS et le contrôle de l’asthme. Bien que le concept de « modification de la maladie » doive être approfondi, ces résultats sont cliniquement significatifs. Ils soutiennent l’utilisation précoce du mépolizumab dans la bonne population de patients pour potentiellement ralentir la progression des lésions des voies respiratoires.12
L’étude MESILICO : preuve de la réduction du remodelage des voies respiratoires sous l’influence de l’inhibition de l’IL-5 par le mépolizumab 12
Chez les patients atteints d’asthme sévère à éosinophiles, l’inflammation chronique peut entraîner des changements structurels permanents dans les voies respiratoires, un phénomène connu sous le nom de remodelage des voies respiratoires.11 Ces changements – tels que l’épaississement de la membrane sous-basale, l’hypertrophie du tissu musculaire lisse et les lésions épithéliales – contribuent à une obstruction irréversible des voies respiratoires et à une perte progressive de la fonction pulmonaire, surtout chez les patients souffrant de formes d’asthme à début tardif et dont la réversibilité est limitée.11
L’étude MESILICO a cherché à savoir si le mépolizumab pouvait également influencer ces changements structurels.12 Dans cette étude multicentrique grecque, 41 patients présentant un asthme sévère à éosinophiles d’apparition tardive et un schéma obstructif ont reçu un traitement par mépolizumab pendant 12 mois en pratique quotidienne. Des échantillons de tissu bronchique ont été analysés avant et après le traitement chez 34 patients. Les résultats ont montré une diminution significative de l’épaisseur de la membrane sous-basale (-17,6 %), de l’épaisseur de la couche musculaire (-26 %), de la surface musculaire (-24,4 %), du nombre d’éosinophiles tissulaires (-47,9 %) et du degré de lésion épithéliale (-38,8%) (tous p < 0,001). Fait remarquable, la réduction de l’épaisseur de la couche musculaire était corrélée positivement à la diminution des éosinophiles dans le tissu sous-muqueux, ce qui indique une relation directe entre l’inflammation éosinophilique et le remodelage tissulaire. Outre ces améliorations histologiques, un bénéfice clinique clair a également été constaté : le nombre d’exacerbations sévères a diminué de 67 % par rapport à l’année précédant le début du traitement par mépolizumab. Une corrélation nette a également été observée entre l’amélioration des paramètres du remodelage des voies respiratoires et les résultats cliniques : une amélioration du contrôle de la maladie (score ACT plus élevé ; Figure 2) ainsi que de la fonction pulmonaire, avec une augmentation de 13,5 % de la valeur de VEMS prédite.12
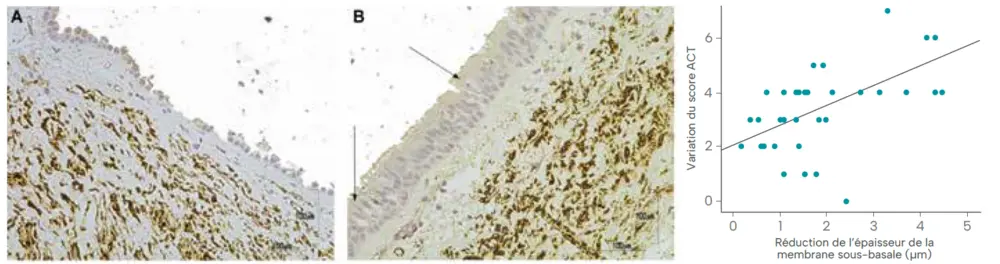
tardif avec obstruction persistante du débit d’air. La figure A (avant le traitement) montre une forte proportion d'épithélium respiratoire
endommagé et dénudé. La figure B (après le traitement par mépolizumab) montre une forte proportion d'épithélium respiratoire normal. Le graphique montre une corrélation positive entre la diminution du score ACT et la réduction de l'épaisseur de la membrane sous-basale.12
“« Les résultats de l’étude MESILICO suggèrent un effet de réduction des marqueurs du remodelage tissulaire bronchique sous mépolizumab. Dans cette étude, le traitement par mépolizumab entraîne en effet une diminution significative de l’épaisseur de la couche musculaire lisse, de l’épaississement sous-épithélial et de l’étendue des lésions épithéliales. Cette restauration histologique semble être étroitement liée à la diminution de l’inflammation éosinophilique dans le tissu des voies respiratoires. Il est à noter que ces effets bénéfiques ont également été observés chez des patients présentant une obstruction peu réversible et un début tardif de la maladie, ce qui contredit l’idée classique selon laquelle le remodelage est irréversible. De plus, les auteurs ont confirmé une amélioration significative de la fonction pulmonaire, du contrôle de l’asthme et une diminution des exacerbations sévères (p<0,001)»12, déclare le professeur Schleich.
Quelle est l’importance d’une intervention thérapeutique précoce dans l’asthme sévère pour obtenir une rémission clinique ?
Professeur Florence Schleich : Une intervention thérapeutique précoce dans l’asthme sévère augmente les chances d’obtenir une super-réponse ou une rémission clinique. Plus nous intervenons tôt – c’est-à-dire avant l’apparition d’un déclin fonctionnel, avant la survenue de changements structurels dans les voies respiratoires (remodelage) et avant l’apparition d’une corticodépendance – plus les chances d’issue favorable sont grandes. Les corticostéroïdes systémiques (CSS) provoquent des effets secondaires graves que nous voulons éviter autant que possible. La plupart des études qui ont analysé les facteurs prédictifs de rémission ou de super-réponse, dont les études réalisées au CHU de Liège, retrouvent une maladie de moins longue durée, l’absence d’usage de CSS en traitement de maintenance et la présence de marqueurs d’inflammation type-2 comme facteurs prédictifs de rémission et de super-réponse.18 L’étude REDES démontre que certaines caractéristiques cliniques de base comme des taux élevés d’éosinophilie systémique, la présence d’une polypose nasale, un meilleur contrôle symptomatique, des doses plus faibles de CSS en maintenance, l’absence de dépression ou de reflux gastro-oesophagien (RGO) sont plus fréquemment liés à l’atteinte de la rémission clinique alors qu’une moins bonne fonction respiratoire de base est associée à des chances amoindries de rémission.6 Nous devons identifier et traiter ces patients asthmatiques sévères avant l’apparition de dommages irréversibles. Les données du registre belge de l’asthme sévère montrent également que l’instauration d’un traitement anti-IL-5 permet de ralentir le déclin fonctionnel respiratoire.19
Qu’est-ce qui, selon vous, rend l’étude MESILICO cliniquement pertinente et innovante ?
Professeur Lieven Dupont : Ce qui rend l’étude MESILICO si particulière, c’est que des bronchoscopies avec biopsies ont été réalisées avant et après un an de traitement par mépolizumab.¹² Ce n’est pas une démarche évidente, mais elle fournit des informations extrêmement précieuses. L’étude MESILICO montre non seulement une diminution du nombre d’éosinophiles dans le sang et les voies respiratoires, mais aussi une réduction des lésions structurelles dans les voies aériennes. On observe ainsi une diminution de l’épaisseur de la membrane basale et moins de dommages épithéliaux — autant de signes clairs d’une inversion du remodelage des voies respiratoires. Cela renforce ma conviction que ce traitement ne se contente pas d’aider nos patients à court terme, mais pourrait également les protéger contre une progression future de la maladie. Ce que cette étude confirme surtout, c’est que le mépolizumab va au-delà du simple contrôle des symptômes. On observe une amélioration cliniquement pertinente au niveau tissulaire, en particulier chez les patients présentant un asthme éosinophilique sévère à début tardif avec un profil obstructif. Les résultats confirment ce que nous ressentons souvent intuitivement en pratique : ce traitement est efficace et agit véritablement sur le processus pathologique sous-jacent.12
Les données de vie réelle avec le mépolizumab confirment une efficacité large et durable dans l’asthme sévère dans l’étude REALITI-A 8-10
Grâce à des études en conditions réelles avec un suivi à long terme, comme l’étude REALITI-A, nous pouvons obtenir un aperçu des effets durables d’un traitement dans la pratique clinique quotidienne. « L’étude REALITI-A était une étude d’observation prospective internationale sur deux ans, dans laquelle 822 adultes atteints d’asthme sévère ont été suivis après l’instauration du mépolizumab (100 mg par voie sous-cutanée, sur décision du médecin traitant). L’étude a comparé les résultats obtenus dans l’année précédant le début du traitement avec ceux observés pendant la période de suivi de deux ans. Le traitement par mépolizumab a été associé à une réduction marquée et durable du nombre d’exacerbations d’asthme cliniquement significatives. Sur l’ensemble de la période de suivi, le nombre d’exacerbations a baissé de 74 %, tandis que le nombre d’exacerbations nécessitant une visite aux urgences/hospitalisation a diminué de 79 %. Le pourcentage de patients qui n’ont présenté aucune exacerbation entraînant une admission aux urgences/hospitalisation est passé de 83 % à 89 %.8 En outre, l’étude REALITI-A a également mis en évidence une diminution significative du traitement d’entretien par corticostéroïdes oraux (CSO). La dose quotidienne médiane de CSO est passée de 10 mg au début de l’étude à 0 mg à la fin de la deuxième année (semaines 101 à 104 ; Figure 3). Le pourcentage de patients qui ont pu arrêter complètement leur traitement d’entretien par CSO a augmenté progressivement à 57 % après deux ans. De plus, 75 % des patients ont réussi à réduire leur dose d’entretien quotidienne d’au moins 50 %. Ces résultats sont impressionnants »8, affirme le professeur Guy Brusselle.
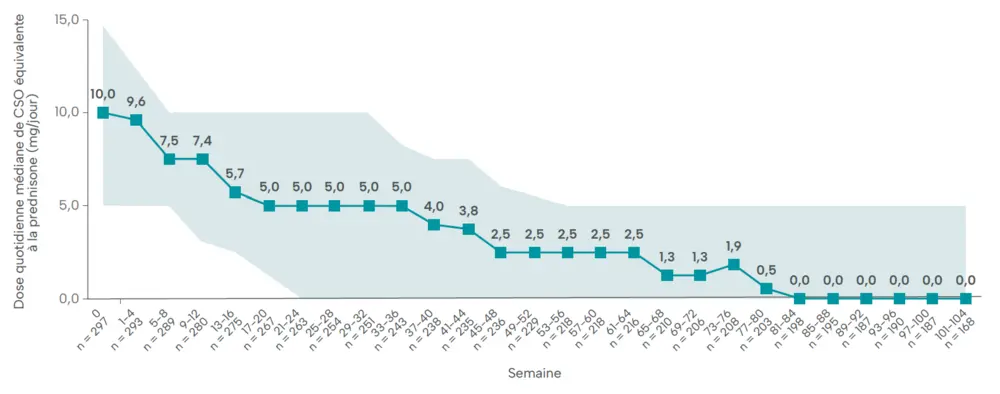
patients atteints d’asthme sévère qui utilisaient des corticostéroïdes oraux en traitement d’entretien au début de l’étude.8
PLe professeur Florence Schleich a souligné l’importance des analyses en vie réelle, telle que REALITI-A, qui montre que les effets du mépolizumab sont maintenus au cours des deux années de suivi. Le mépolizumab permet une diminution du nombre d’exacerbations cliniquement significatives et de la proportion de patients recevant un traitement de maintenance par CSS mais aussi une amélioration des paramètres fonctionnels respiratoires et du contrôle symptomatique, effets également observés dans la cohorte du CHU de Liège.9,10,20
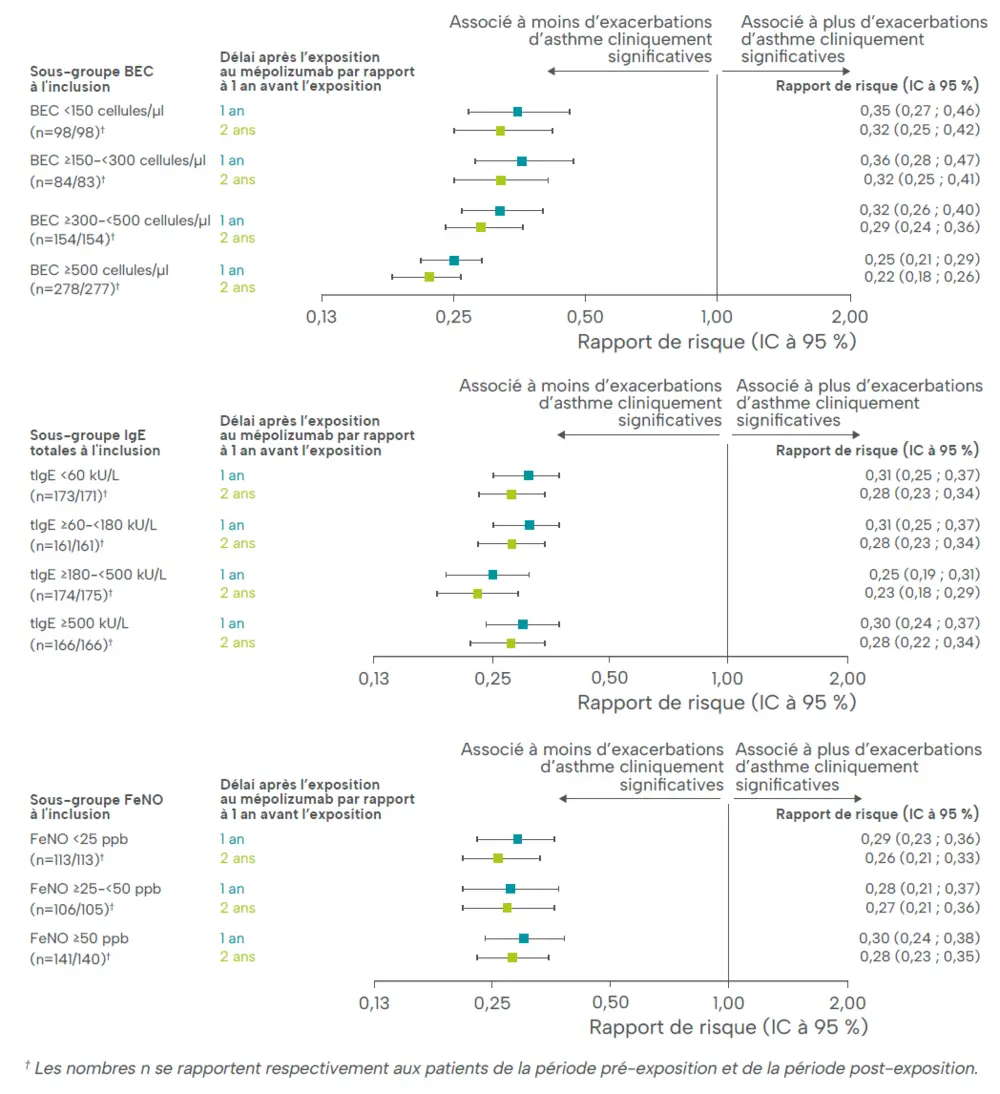
De plus, dans REALITI-A, le mépolizumab réduit les exacerbations indépendamment des valeurs initiales d’éosinophiles sanguins, d’IgE totales ou de FeNO, avec cependant des réductions d’exacerbations les plus élevées pour les patients présentant des taux élevés d’éosinophiles systémiques et d’IgE (Figure 4). Une approche précoce et ciblée avec un médicament biologique tel que le mépolizumab fait donc la différence à long terme, tant en ce qui concerne la progression de la maladie que la réduction des effets secondaires liés à l’usage des corticostéroïdes systémiques.9,10
« Chez les patients ayant recours de manière récurrente aux corticostéroïdes oraux – pensez à deux cures ou plus par an – il faut réellement envisager de manière précoce l’introduction d’un médicament biologique. Plus on attend, plus le risque de dommages irréversibles des voies respiratoires augmente, et la probabilité de rémission diminue. Grâce aux thérapies biologiques, le fatalisme qui entourait autrefois l’asthme sévère n’a plus lieu d’être : nous disposons aujourd’hui d’options réelles qui font la différence, à condition d’intervenir à temps. Mon message à tous les prestataires de soins de première ligne est donc de repérer au plus vite les patient souffrant potentiellement d’asthme sévère et de les orienter rapidement vers un
spécialiste », déclare le professeur Lieven Dupont.9-10
La rémission comme nouvel objectif thérapeutique dans l’asthme sévère : le mépolizumab rend cela possible
La rémission clinique pendant le traitement de l’asthme sévère est un objectif thérapeutique ambitieux. Dans une analyse posthoc de l’étude REALITI-A, le pourcentage de patients atteints d’asthme sévère, qui ont obtenu une rémission clinique au début de l’étude, après 52 semaines et après 104 semaines de traitement par mépolizumab a été analysé.13 La rémission clinique a été définie comme suit : 1) absence de traitement d’entretien par corticostéroïdes oraux (CSO) ; 2) absence d’exacerbations nécessitant un traitement par CSO et/ou une visite aux urgences ou une hospitalisation ; 3) score < 1,5 à l’Asthma Control Questionnaire-5 (ACQ-5) et 4) absence de détérioration de la fonction pulmonaire. Dans cette analyse post-hoc, les patients étaient en rémission clinique lorsqu’ils répondaient aux 4 composantes de cette définition.13 Le professeur Guy Brusselle a résumé les résultats comme suit : « Environ un tiers des patients atteints d’asthme sévère ont obtenu une rémission clinique après 1 et 2 ans de traitement par mépolizumab. En utilisant le mépolizumab de manière continue, un plus grand nombre de patients ont obtenu une rémission clinique après 2 ans. N’arrêtez donc pas le traitement trop tôt. »13
« Si la rémission sous traitement est un objectif séduisant dans l’asthme sévère à éosinophiles, objectif atteint dans environ un tiers des cas, nous devons prendre le patient dans son ensemble pour en prédire les chances, en tenant compte de ses comorbidités, de l’utilisation des CSS en traitement de maintenance et de l’intensité de l’inflammation de type 2. Les analyses du UK Severe Asthma Registry (UKSAR) montrent que la probabilité de rémission diminue de 14 % par décennie supplémentaire de maladie. Cela confirme ce que nous observons depuis longtemps dans la pratique : plus on traite tôt, meilleure est la probabilité de rémission.14 L’étude REDES et UKSAR soulignent l’importance de prendre en compte les comorbidités. Alors que la rhinosinusite chronique avec polypose est associée à un bon pronostic, la présence d’une obésité, d’une anxiété et dépression, d’un RGO ou d’une histoire tabagique sont associés à des chances réduites de rémission.6,14 Par ailleurs, les patients présentant une inflammation de type 2 importante atteignent plus souvent le statut rémission alors qu’un traitement de maintenance par CSS en réduit fortement les chances.15 Ces données plaident pour une approche précoce et personnalisée des patients à risque, avec endotype de type 2 et histoire d’exacerbations répétées avec pour objectif ambitieux la rémission, soit l’absence durable des symptômes, d’exacerbation et de recours aux CSS et une normalisation ou optimalisation de la fonction respiratoire16 », explique
le professeur Florence Schleich. Ces données montrent qu’un traitement anticipé et continu par le mépolizumab est crucial pour maximiser les chances de rémission clinique chez les patients appropriés, même si cette rémission n’est obtenue que progressivement.
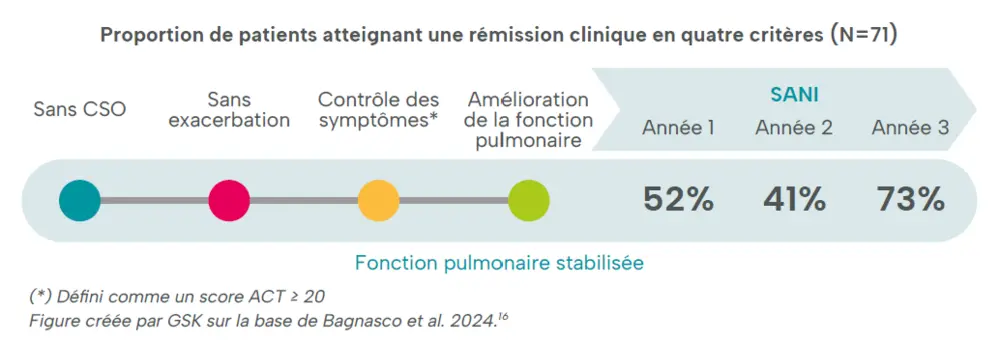
Une étude italienne qui a suivi des patients pendant trois ans a montré que la rémission n’était pas nécessairement immédiate.16 Ainsi, 22 % des patients qui n’avaient obtenu qu’une rémission partielle après un an sont parvenus à une rémission complète la troisième année (Figure 5). Cela souligne l’importance d’une thérapie continue, même en cas de progression lente des résultats du traitement.16 Le professeur Lieven Dupont l’a résumé ainsi : « En visant la rémission clinique, nous plaçons volontairement la barre plus haut : nous ne voulons pas seulement réduire les exacerbations ou le recours aux corticostéroïdes oraux, mais aussi obtenir une bonne fonction pulmonaire et un contrôle optimal des symptômes. Bien sûr, tous les patients n’atteignent pas cet idéal. En pratique, cela concerne environ 30 à 40 % des cas, ce qui est en réalité assez élevé comparé à d’autres maladies chroniques. L’essentiel, c’est que le concept de rémission nous aide à changer de perspective : passer d’une simple gestion des symptômes à un contrôle plus ambitieux et global de l’asthme sévère. »13-16
Conclusion
L’inflammation de type 2 est à l’origine des lésions des voies respiratoires, de la progression de la maladie et du remodelage dans l’asthme sévère. L’IL-5 joue un rôle central à cet égard, dont les effets vont au-delà de la simple activation éosinophilique. L’étude MESILICO révèle que l’inhibition de l’IL-5 par le mépolizumab peut réduire les changements structurels dans les voies respiratoires, ce qui a un impact clinique positif.12 Cette action multidirectionnelle sur différents processus pathologiques – de l’inflammation au remodelage – souligne le potentiel de modification de la maladie du mépolizumab. Les données du monde réel, comme les études REDES et REALITI-A, confirment que ces effets se maintiennent également dans la pratique clinique.6-10 Par ailleurs, plusieurs analyses montrent que, dans un groupe de patients bien sélectionnés, un tiers des patients atteint la rémission clinique après un traitement prolongé par mépolizumab : un objectif final ambitieux mais réaliste, qui plaide en faveur
d’une thérapie précoce et soutenue.13-16
Dr G. Fonteyn
Rédaction: laréférence médicale - Article en collaboration avec GSK.

Réimpression d’un article paru dans La référence médicale,
n° 5/2025 (mai/juin). À consulter via www.reference-medicale.be
Références
1. Ortega HGLM, et al. Mepolizumab treatment in patients with severe eosinophilic asthma. The New England Journal of Medicine 2014; 371 (13):1198-1207.
2. Bel EH, et al. Oral glucocorticoid-sparing effect of mepolizumab in eosinophilic asthma. The New England Journal of Medicine 2014; 371 (13):1189-1197.
3. Chupp GL, et al. Efficacy of mepolizumab add-on therapy on health-related quality of life and markers of asthma control in severe eosinophilic asthma (MUSCA): a randomised, double-blind, placebocontrolled, parallel-group, multicentre, phase 3b trial. Lancet Respiratory Medicine 2017;5 (5): 390-400.
4. Nucala. Summary of product characteristics.
5. Brown T, et al. Randomised controlled trials in severe asthma: selection by phenotype or stereotype. European Respiratory Journal 2018; 52 (6): 1801444.
6. Domingo Ribas C, et al. REal worlD Effectiveness and Safety of Mepolizumab in a Multicentric Spanish Cohort of Asthma Patients Stratified by Eosinophils: The REDES Study. Drugs 2021; 81: 1763-1774.
7. Buchheit K, et al. Interleukin-5 as a pleiotropic cytokine orchestrating airway type 2 inflammation: Effects on and beyond eosinophils. Allergy 2024; 79: 2662-2679.
8. Caruso C, et al. Prospective REALITI-A Study. 2-Year Real-World Benefits of Mepolizumab in Severe Asthma. CHEST Pulmonary 2025; 3 (1): 100107.
9. Lee J, et al. Mepolizumab Improves and Sustains Clinical Benefits in Patients With Severe Asthma, Independent of IgE and FeNO at Baseline: Real-world Analysis of REALITI-A Results at 2 Years. AAAAI 2025. February 28 - March 3, 2025. San Diego, USA.
10. Liu M, et al. Mepolizumab Improves and Sustains Clinical Benefits in Patients With Severe Asthma, Independent of Blood Eosinophil Count at Baseline: Real-World Analysis of REALITI-A Results at 2 Years. AAAAI 2025. February 28 - March 3, 2025. San Diego, USA.
11. Hsieh A, et al. Airway remodeling heterogeneity in asthma and its relationship to disease outcomes. Frontiers in Physiology 2023; 14: 1113100.
12. Domvri K, et al. Effect of mepolizumab in airway remodeling in patients with late-onset severe asthma with an eosinophilic phenotype. Journal of Allergy and Clinical Immunology 2025; 155: 425-435.
13. Brusselle G, et al. Clinical remission achievement in severe asthma following mepolizumab treatment: results from the REALITI-A study at 2 years. Poster 203 presented at: American Thoracic Society Meeting; May 19-24, 2023; Washington, DC, USA.
14. McDowell PJ, et al. Clinical remission in severe asthma with biologic therapy: an analysis from the UK Severe Asthma Registry. European Respiratory Journal 2023; 62: 2300819.
15. Pavord I, et al. Remission outcomes in severe eosinophilic asthma with mepolizumab therapy: Analysis of the REDES study. Frontiers in Immunology 2023; 14: 1150162.
16. Bagnasco D, et al. Evaluation of Clinical Remission in Best-Performing Severe Asthmatic Patients Treated for Three Years with Mepolizumab. Biomedicines 2024; 12: 960.
17. Bagnasco D, et al. The role of IL-5 in type 2 inflammatory diseases. EMJ 2024; 9 (4): 62-72.
18. Vervier J, et al. Concept of remission in severe asthma. Revue Médicale de Liège 2024; 79 (4): 241-247.
19. Graff S, et al. Anti-Interleukin-5 Therapy Is Associated with Attenuated Lung Function Decline in Severe Eosinophilic Asthma Patients From the Belgian Sever Asthma Registry. Journal of Allergy and Clinical Immunology – In Practice 2022; 10 (02): 467-477.
20. Schleich F, et al. Real-word experience with mepolizumab: Does it deliver what it has promised? Clinical and Experimental Allergy 2020; 50 (6): 687- 695. PM-BE-MPL-RPNT-250006 – Juillet 2025

