Radiologie interventionnelle
La cryoablation se profile comme le traitement du futur pour les tumeurs desmoïdes
Le 5 mars, l’équipe de radiologie interventionnelle du CHU Helora (site Jolimont) a réalisé sa première cryoablation d’une tumeur desmoïde. Le patient va bien et est ravi. Le patient va bien et est ravi. Mini-invasive et réplicable au besoin, le Dr Raphaël Lévêque, radiologue interventionnel, évoque une méthode amenée à se généraliser en première intention.
Le journal du Médecin : Avant d’évoquer la technique, pourquoi entend-on si peu souvent parler des tumeurs desmoïdes ?
Dr Raphaël Lévêque : En réalité, c’est une tumeur assez rare : on parle de 2 à 3 cas par million d’habitants et par an. Cela dit, je pense que c’est probablement un peu sous-estimé, parce que j’en entends de plus en plus souvent parler, notamment avec le développement de traitements percutanés.
Les desmoïdes sont des tumeurs qu’on dit bénignes : elles ne sont pas infiltrantes comme certains sarcomes, mais elles peuvent être très agressives. D’ailleurs, on les appelle aussi fibromatose agressive. Certaines ne bougent pas et ne provoquent pas de douleurs (ou provoquent des douleurs qui ne gênent pas) et qu’on peut simplement surveiller. Mais d’autres grossissent très vite, et, là, ça devient problématique parce que la tumeur va pousser sur les structures adjacentes. C’est à ce moment-là que les douleurs apparaissent, et qu’au bout d’un moment, il faut intervenir.
Quelques aiguilles pour du mini-invasif
À ce stade, quelle est l’approche classique pour intervenir ?
Le problème, même si c’est une tumeur bénigne, c’est qu’elle récidive très rapidement. Sur le plan chirurgical, quand on intervient, c’est souvent déjà tard et c’est déjà assez volumineux. Pour que ce soit efficace, la chirurgie peut être très délabrante, selon l’endroit où se trouve la tumeur.
Du coup, des techniques se sont développées, davantage en percutané. Et depuis quelques années, il y a surtout la cryoablation, qui, d’après les études, s’est révélée aussi efficace que la chirurgie, sans le versant délabrant.
Plus largement, toutes les techniques percutanées de thermoablation sont en plein essor, parce qu’on dispose maintenant de plus en plus d’études, y compris dans de grandes revues, qui montrent des résultats de non-infériorité.
Concrètement fonctionne la cryoablation ?
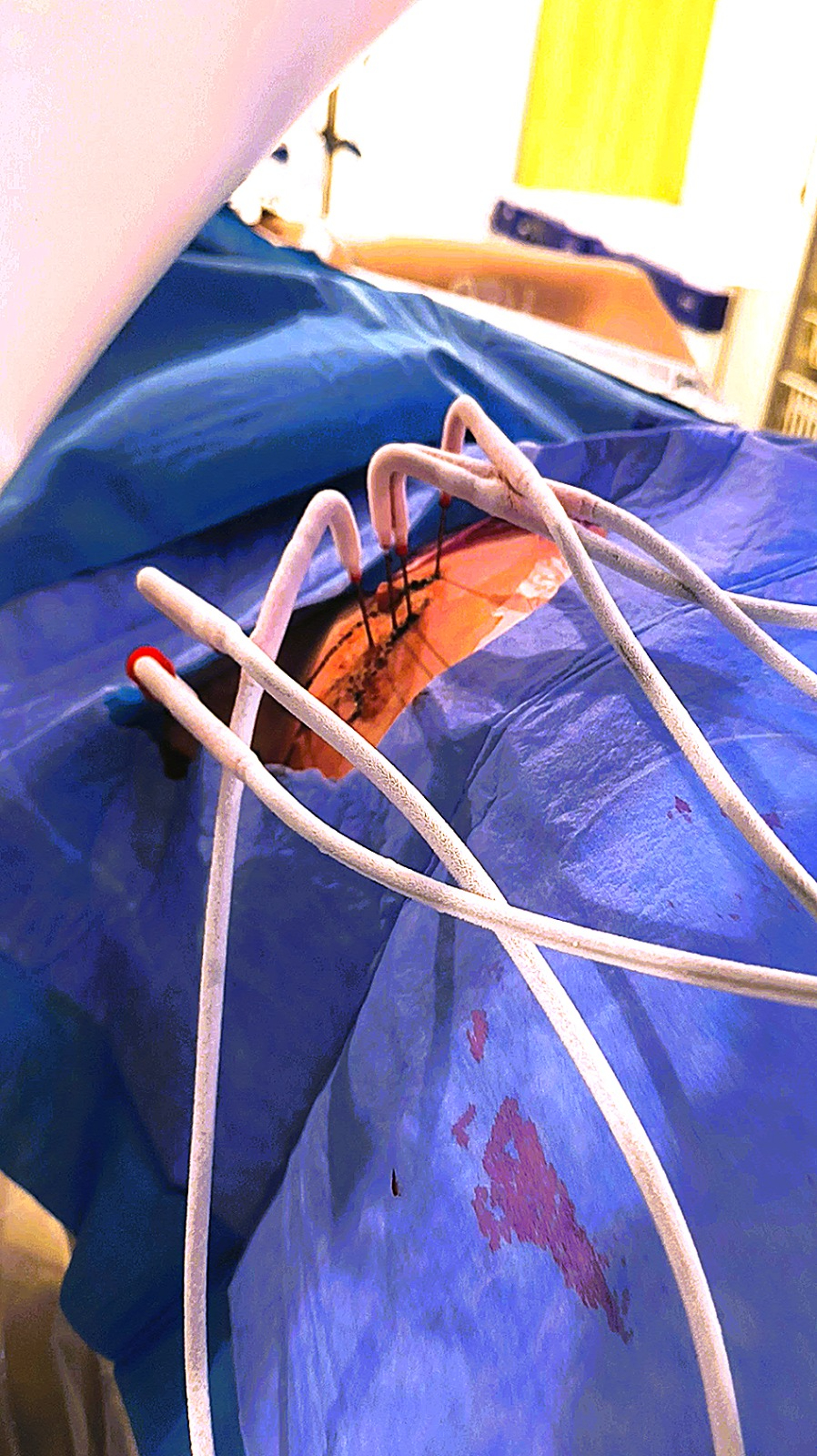
On fait l’intervention sous scanner, sous sédation ou anesthésie générale, pour être sûr que le patient ne bouge pas. On repère la lésion (chez le patient opéré au début du mois, il s’agissait d’une lésion de la paroi thoracique) et on y place plusieurs aiguilles qui seront traversées par un gaz, l’argon, qui s’y décompresse provoquera un froid intense.
L’idée, c’est que plus on met d’aiguilles, plus on peut faire un « glaçon » important. Et selon le type d’aiguilles et leur puissance, on peut aussi donner une forme à ce glaçon. Il y a donc toute une phase de planification juste avant l’acte. On voit d’ailleurs émerger de plus en plus de logiciels (parfois avec de l’IA) qui permettent de faire des reconstructions en 3D et de simuler le positionnement optimal des aiguilles pour obtenir le glaçon souhaité, avec nos marges. Au CHU Helora, nous faisons déjà ce type de planification, y compris pour d’autres indications : tumeurs du rein, tumeurs hépatiques, etc. Beaucoup de start-up se lancent également là-dedans… On voit même arriver des systèmes robotisés !
Après la phase de planification, sous scanner, il faut le temps de bien positionner les aiguilles. Cela prend un peu de temps : disons qu’en une heure, les aiguilles sont correctement en place. Ensuite, on lance les cycles de froid et de chaud, qui durent chacun environ une demi-heure.
« Ice Ball »
Comment la congélation parvient-elle à détruire la tumeur ?
Le bout des aiguilles devient très froid : il forme un glaçon, de l’ordre de -40°C. Puis on réchauffe un peu pour faire fondre, et cette alternance amplifie les phénomènes d’entrée et de sortie d’eau au niveau cellulaire, ce qui provoque la destruction des cellules. C’est ce qui explique l’efficacité du traitement et entraîne une apoptose. Les cellules « explosent », en quelque sorte. Celles qui survivent partiellement peuvent aussi être détruites par ces variations liées à l’osmose.
Ensuite, on réalise un deuxième cycle, on reforme un second glaçon, puis on retire le matériel. Le corps étant à 37 °C, tout cela va fondre progressivement. Sur l’imagerie, ce qui reste immédiatement visible, c’est cette « boule » correspondant à la zone gelée, qui se résorbera finalement. Au total, si tout se passe bien, en deux heures, c’est réglé.
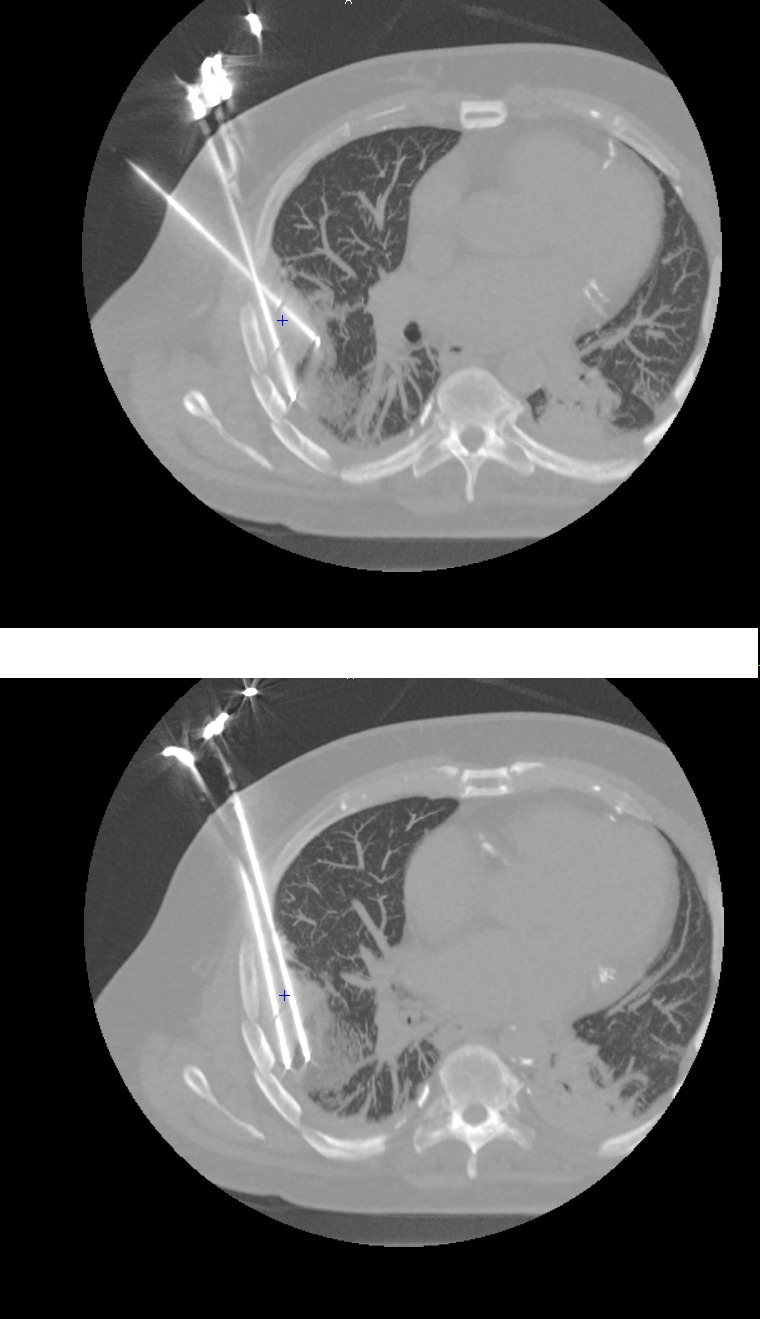
Après, on fait un suivi par imagerie à trois et à six mois, pour vérifier si le traitement a été suffisant ou s’il faut y revenir. Logiquement, les cellules dans la zone traitée sont mortes : on arrive à obtenir une bonne marge, et surtout on épargne les structures adjacentes (les nerfs, les vaisseaux) parce qu’on voit très bien où l’on va. Dans un cas comme celui de notre premier patient, chirurgicalement, il aurait probablement fallu enlever une côte, voire une partie de la plèvre : c’aurait été une opération très délabrante.
Cela semble être le grand avantage de la cryothérapie…
L’avantage principal, par rapport à la chirurgie, c’est qu’on peut intervenir de façon mini-invasive.
L’autre avantage, c’est qu’on crée une sorte de « boule de glace » (ice ball) que l’on voit très bien au scanner : on visualise précisément la zone traitée et on peut contrôler les marges.
Surtout, on peut également répéter le geste autant de fois que nécessaire, puisque ce sont de petites aiguilles. On ne met même pas de points ensuite : on place les aiguilles, on fait l’intervention, et le patient rentre généralement le lendemain (on garde quand même une nuit en observation). Et s’il y a un souci, on peut réintervenir sans problème. Même quand les tumeurs sont très volumineuses, on peut aussi prévoir un traitement en plusieurs séances.
C’est d’ailleurs un point important : après une chirurgie, si on doit retourner au même endroit, il y a de la fibrose, des adhérences (appelée « synéchies » dans l’utérus) et souvent les chirurgiens n’aiment pas réintervenir sur une zone déjà opérée ou irradiée, parce que tout est remanié. Ici, au contraire, on peut traiter une zone et y revenir sans que cela empêche, ensuite, une autre option thérapeutique.
Au final, à mon avis, cela devrait être envisagé en première intention, de manière de plus en plus systématique. Je pense d’ailleurs que c’est ce qui va se faire progressivement.
Désormais remboursée par l’INAMI
Le traitement coûte-t-il cher au patient et à l’hôpital ?
La situation évolue ! On a vu notre patient en 2025. La biopsie montrait que la tumeur grossissait, mais de manière raisonnable, donc on a préféré attendre. Le patient n’était pas pressé de se faire opérer, et on avait l’information qu’un remboursement de l’INAMI allait arriver. Une aiguille coûte de l’ordre de 1.200 euros. Si on doit en mettre cinq et que ce n’est pas remboursé, la pharmacie vous tape sur les doigts. En universitaire, on peut parfois se permettre certaines choses, mais ici, l’enjeu, c’est que ce soit un traitement accessible à tous.
Depuis le 1er février 2026, l’INAMI a donc mis en place un remboursement des aiguilles de cryoablation dans le cadre de la tumeur desmoïde, dans les hôpitaux conventionnés dont fait partie le site de Jolimont. Financièrement c’est beaucoup plus avantageux que la chirurgie. Les patients ne restent pas hospitalisés longtemps, ils récupèrent plus vite et peuvent reprendre leurs activités.
Bien sûr, il y a une condition : il faut que ce soit réalisé dans des centres spécialisés. C’est d’ailleurs pour ça que l’INAMI a instauré, en novembre 2024, des conventions pour la thermoablation et l’ablation percutanée. En principe, un nombre limité de centres bénéficient du code de remboursement, avec des critères, un volume minimum d’interventions, une garde interventionnelle pour gérer les éventuelles complications, et des contrôles. L’objectif, c’est d’éviter que « tout le monde » s’y mette sans expérience.
Pourquoi ne traite-t-on pas tous les cancers solides avec la cryoablation ?
Il faut encore attendre les données scientifiques, même si elles sont de plus en plus nombreuses. Et c’est justement pour ça que ces techniques s’imposent progressivement lors des réunions multidisciplinaires.
Après, il ne faut pas se mentir : même si c’est mini-invasif, ça reste invasif. On introduit des aiguilles. Donc, dans certains cas (notamment quand il s’agit d’une petite lésion bien localisée) on peut encore privilégier une chirurgie ou une radiothérapie. En tant que radiologue interventionnel, je connais la technique, je sais qu’il y a très peu de complications, donc j’ai tendance à considérer que c’est une bonne option.
Rien que pour le foie, comme je le disais, il y a une étude sortie en 2024 qui montrait que, pour les métastases colorectales, la thermoablation était non inférieure à la chirurgie, avec des patients qui peuvent sortir dès le lendemain. Et il y a aussi une étude danoise publiée en 2025 qui montrait que, pour certaines tumeurs du rein, c’était également comparable à la chirurgie.
Maintenant, il y a des situations où c’est plus compliqué. Par exemple, si la tumeur est très proche d’un vaisseau, cela peut être plus délicat : dans ces cas-là, on peut privilégier la chirurgie, surtout si elle est considérée comme « facile » et qu’on peut obtenir une vraie marge. Parce que même si, en imagerie, on visualise nos marges, on n’a pas la preuve histologique qu’on a traité « en marge saine ».
Donc il y a encore des indications où la chirurgie ou la radiothérapie gardent toute leur place. Et c’est pour ça que la décision est forcément multidisciplinaire : elle se prend avec le chirurgien, l’oncologue, et bien sûr avec le patient, parce que le patient doit pouvoir choisir la stratégie qui lui convient.
