Belang van vaccinatie tijdens de zwangerschap met opkomende infectieziekten in het vizier
EAPS-CONGRES 2025 Tijdens het recente congres van de European Academy of Paediatric Societies, deelde prof. dr. Beate Kampmann haar inzichten over de vaccinatie van zwangere vrouwen.
Kampmann is hoogleraar Global Health aan de Charité (Berlijn) en Pediatrische Infectieziekten aan de London School of Hygiene and Tropical Medicine. Zij geldt wereldwijd als een vooraanstaand expert op het gebied van pediatrische infectieziekten en immuniteit, met een specifieke focus op maternale vaccinatie. Vaccinatie tijdens de zwangerschap is cruciaal voor de preventie van ziekten die ernstig kunnen verlopen voor zowel de moeder als de pasgeborene, zeker in de periode voordat de baby zelf gevaccineerd kan worden.
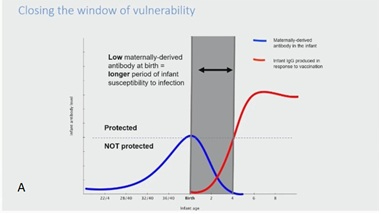
Via de placenta worden IgG-antilichamen overgedragen naar de foetus. Deze passieve immuniteit fungeert als een 'brug' tot de kindervaccinaties starten (figuur A).
Door de moeder te vaccineren, bereiken hogere concentraties antilichamen de foetus, waardoor de kwetsbare periode na de geboorte wordt verkort (figuur B). Zwangerschapsvaccinatie is geen nieuw concept; vaccinaties tegen tetanus, kinkhoest en griep zijn al jaren de standaard.
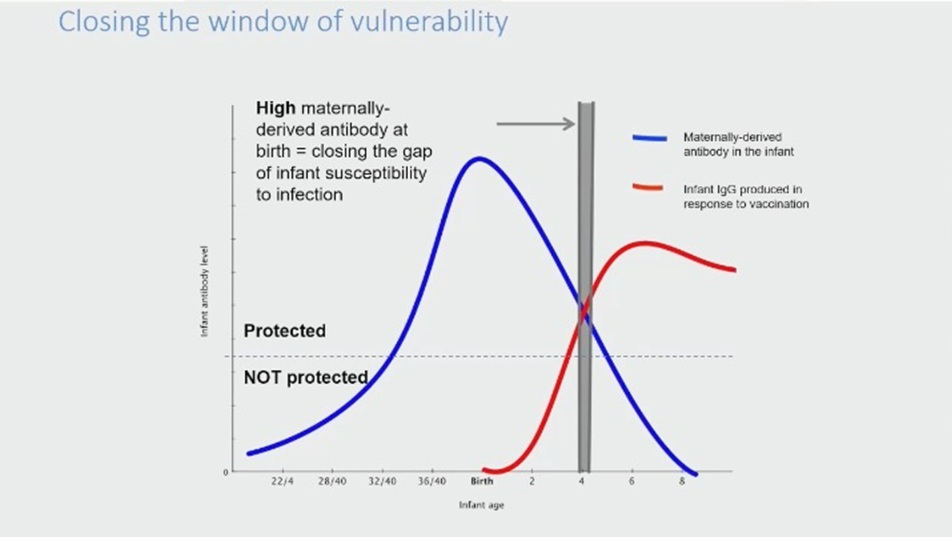
(aangepast van presentatie prof. Kampmann, EAPS Congress 2025).
Recent werd bovendien een RSV-vaccin voor zwangere vrouwen goedgekeurd.(1) Meer aandacht voor dit thema is essentieel, zeker met het oog op opkomende ziekteverwekkers zoals chikungunya, lassakoorts en mpox. Hoewel zwangere vrouwen traditioneel werden uitgesloten van klinische studies, groeit het besef dat onderzoek naar veiligheid en doeltreffendheid in deze groep noodzakelijk is om hen niet uit te sluiten van toekomstige vaccinatiecampagnes.
Lessen uit de covid-19-pandemie
De covid-19-pandemie onderstreepte het belang van data over zwangere vrouwen. Omdat zij niet waren opgenomen in de initiële klinische studies, werden de vaccins tijdens de implementatie gebruikt zonder voorafgaande specifieke data voor deze doelgroep. Veiligheidsgegevens werden pas achteraf verzameld via geneesmiddelenbewaking. Deze suboptimale situatie leidde tot verwarring en uiteenlopend beleid tussen landen.
Het heeft er echter wel toe geleid dat regelgevende instanties hun richtlijnen hebben aangepast. Waar het tot 2018 de standaard was om zwangere vrouwen uit te sluiten van klinisch onderzoek, wordt nu aanbevolen hen juist te betrekken, mits er voldoende preklinische en preliminaire veiligheidsdata beschikbaar zijn.(2,3)
Vaccinatie in de context van opkomende infectieziekten
Chikungunya: Tot voor kort werd dit in Europa vooral gezien als importziekte, maar inmiddels zijn er lokale uitbraken gemeld in Frankrijk en Italië.(4) De tijgermug, die het virus verspreidt, vestigt zich structureel in Europa. Bij de moeder verloopt de ziekte meestal zonder specifieke complicaties, maar bij een infectie rond de bevalling loopt het risico op overdracht naar het kind op tot 50%. Neonatale infectie kan leiden tot sepsis en neurologische complicaties; 28% tot 50% van deze kinderen houdt er een neurologische achterstand aan over. Hoewel er twee vaccins beschikbaar zijn in de EU, worden deze momenteel niet aanbevolen tijdens de zwangerschap omdat zwangere vrouwen niet in de studies werden opgenomen.(5,6) Post-marketing surveillance is daarom essentieel om data te verzamelen van vrouwen die onverwacht zwanger bleken tijdens vaccinatie.
Lassakoorts: Deze virale hemorragische koorts is endemisch in West-Afrika en wordt verspreid via ratten of menselijk contact. Zwangere vrouwen en foetussen zijn extreem kwetsbaar voor het virus, met een zeer hoog risico op overlijden.(7) Verschillende vaccins zijn in ontwikkeling.(8) De meest geavanceerde kandidaat is echter gebaseerd op een replicerende virale vector, wat minder geschikt is voor zwangere vrouwen. Toch zou vaccinatie met dit vaccin in kritieke situaties aangewezen kunnen zijn.
Mpox: Net als pokken verhoogt mpox het risico op ernstige ziekte bij de moeder, miskramen en doodgeboortes(9). Er is een vaccin, maar ook hier ontbreken klinische data voor zwangere vrouwen.(10) Een fase 3-studie in de Democratische Republiek Congo is momenteel lopende.
Ebola: Net als bij covid-19 werden ebolavaccins tijdens uitbraken bij zwangere vrouwen gebruikt zonder voorafgaande klinische data. Ebola is bijna altijd fataal voor de foetus en verhoogt de moedersterfte aanzienlijk.(11) Inmiddels zijn er twee vaccins beschikbaar.(12,13) Dankzij specifieke protocollen tijdens de uitbraak in West-Afrika konden voor één van de twee vaccins toch geruststellende veiligheidsgegevens gegenereerd worden. Ook recent gepubliceerde fase 3-data van het tweede vaccin bij meer dan 2.000 zwangere vrouwen toonden geen onverwachte bijwerkingen bij moeder of kind.(14,15)
Hulpmiddelen voor veiligheidsmonitoring
Prof. Kampmann benadrukt drie belangrijke pijlers voor de studie van maternale vaccinatie:
1) evaluatie van de noodzaak,
2) verzamelen van bewijs voor effectiviteit en veiligheid,
en 3) beleidsimplementatie.
Voor veiligheid moet niet alleen naar bijwerkingen bij de moeder worden gekeken, maar ook naar zwangerschapsuitkomsten (zoals miskramen), geboorte-uitkomsten (zoals vroeggeboorte) en de gezondheid van het kind op lange termijn.
Om effecten correct te beoordelen, zijn betrouwbare epidemiologische achtergrondgegevens (hoe vaak komen deze complicaties normaal gesproken voor?) cruciaal. Dit vereist internationale samenwerking. Initiatieven zoals het GAIA-consortium en nieuwe aanbevelingen van de WHO helpen om data geharmoniseerd te verzamelen.(16-19)
Tot slot wijst prof. Kampmann op de noodzaak om de kennis over zwangerschapsvaccinatie te vergroten, zowel bij zorgverleners als bij het publiek. Er is een maatschappelijk debat nodig over de acceptatie van levensreddende vaccins waarvan de klinische data in een vroeg stadium nog beperkt kunnen zijn. Zij meent dat we als maatschappij de plicht hebben om hier al in een vroeg stadium van de vaccinontwikkeling over na te denken.
Referenties:
1. https://www.ema.europa.eu/en/medicines/human/EPAR/abrysvo.
2. Krubiner CB, Faden RR, Karron RA, Little MO, Lyerly AD, Abramson JS, Beigi RH, Cravioto AR, Durbin AP, Gellin BG, Gupta SB, Kaslow DC, Kochhar S, Luna F, Saenz C, Sheffield JS, Tindana PO; PREVENT Working Group. Pregnant women & vaccines against emerging epidemic threats: Ethics guidance for preparedness, research, and response. Vaccine. 2021 Jan 3;39(1):85-120. doi: 10.1016/j.vaccine.2019.01.011. Epub 2019 May 3. PMID: 31060949; PMCID: PMC7735377.
3. https://www.fda.gov/drugs/development-resources/division-pediatrics-and-maternal-health-clinical-trials-pregnant-women
4. https://www.ecdc.europa.eu/en/chikungunya-virus-disease
5. https://www.ema.europa.eu/en/medicines/human/EPAR/vimkunya
6. https://www.ema.europa.eu/en/medicines/human/EPAR/ixchiq
7. Kayem ND, Benson C, Aye CYL, Barker S, Tome M, Kennedy S, Ariana P, Horby P. Lassa fever in pregnancy: a systematic review and meta-analysis. Trans R Soc Trop Med Hyg. 2020 May 7;114(5):385-396. doi: 10.1093/trstmh/traa011. PMID: 32125412; PMCID: PMC7197258.
8. https://cepi.net/lassa-fever
9. Nachega JB, Mohr EL, Dashraath P, Mbala-Kingebeni P, Anderson JR, Myer L, Gandhi M, Baud D, Mofenson LM, Muyembe-Tamfum JJ; Mpox Research Consortium (MpoxReC). Mpox in Pregnancy - Risks, Vertical Transmission, Prevention, and Treatment. N Engl J Med. 2024 Oct 10;391(14):1267-1270. doi: 10.1056/NEJMp2410045. Epub 2024 Aug 28. PMID: 39197097.
10. https://www.ema.europa.eu/en/medicines/human/EPAR/imvanex
11. Foeller ME, Carvalho Ribeiro do Valle C, Foeller TM, Oladapo OT, Roos E, Thorson AE. Pregnancy and breastfeeding in the context of Ebola: a systematic review. Lancet Infect Dis. 2020 Jul;20(7):e149-e158. doi: 10.1016/S1473-3099(20)30194-8. Epub 2020 May 6. Erratum in: Lancet Infect Dis. 2020 Aug;20(8):e180. doi: 10.1016/S1473-3099(20)30431-X. Erratum in: Lancet Infect Dis. 2021 Apr;21(4):e81. doi: 10.1016/S1473-3099(21)00138-9. PMID: 32595045.
12. https://www.ema.europa.eu/en/medicines/human/EPAR/ervebo
13. https://www.ema.europa.eu/en/medicines/human/EPAR/zabdeno
14. Nyombayire J, Ingabire R, Mazzei A, Sharkey T, Umuhoza C, Mukamuyango J, Allen S, Tichacek A, Parker R, Wall KM, Katwere M, Keshinro B, Gaddah A, Wang Y, Forcheh CA, McLean C, Oriol-Mathieu V, Luhn K, Robinson C, Karita E. Heterologous two-dose Ebola vaccine regimen in pregnant women in Rwanda: a randomized controlled phase 3 trial. Nat Med. 2025 Nov;31(11):3899-3906. doi: 10.1038/s41591-025-03932-z. Epub 2025 Sep 8. PMID: 40921806; PMCID: PMC12618248.
15. Kampmann, B., Hucko, A. Ebola vaccine safe for mothers and infants. Nat Med 31, 3618–3619 (2025). https://doi.org/10.1038/s41591-025-04000-2
16. Davies HG, Bowman C, Watson G, Dodd C, Jones CE, Munoz FM, Heath PT, Cutland CL, Le Doare K. Standardizing case definitions for monitoring the safety of maternal vaccines globally: GAIA definitions, a review of progress to date. Int J Gynaecol Obstet. 2023 Jul;162(1):29-38. doi: 10.1002/ijgo.14843. Epub 2023 May 16. PMID: 37194339.
17. Stuurman AL, Sharan A, Jahagirdar S, Elango V, Riera-Montes M, Kashyap N, Biccler J, Poluru R, Arora N, Mathai M, Mangtani P, DeVlieger H, Anderson S, Whitaker B, Wong HL, Cutland C, Guillard Maure C; WHO GVS MCC Sites. WHO global vaccine safety multi-country collaboration project on safety in pregnancy: Assessing the level of diagnostic certainty using standardized case definitions for perinatal and neonatal outcomes and maternal immunization. Vaccine X. 2021 Nov 3;9:100123. doi: 10.1016/j.jvacx.2021.100123. PMID: 34825164; PMCID: PMC8605263.
18. https://www.who.int/publications/i/item/WHO-2019-nCoV-pregnancy-and-neonates-2022.
19. Munoz FM, Kampmann B, Stergachis A, Chaudhary M, Cutland CL, Khalil A, Gentile A, Jones CE, Marshall H, Sevene E, Darko DM, Swamy G, Hyde TB, Voss G, Muelen AS. A template tool for the evaluation of vaccines for emerging pathogens to be used for pregnant and breast-feeding women. Vaccine. 2025 Aug 30;62:127513. doi: 10.1016/j.vaccine.2025.127513. Epub 2025 Jul 18. PMID: 40683139.
